Regardez maintenant : Quelles sont les différences entre les acides et les bases ?
Voici 10 faits sur les acides et les bases pour vous aider à vous informer sur les acides, les bases et le pH, ainsi qu’un tableau de comparaison.
- Tout liquide aqueux (à base d’eau) peut être classé comme acide, base ou neutre. Les huiles et autres liquides non aqueux ne sont ni des acides ni des bases.
- Il existe différentes définitions des acides et des bases, mais les acides peuvent accepter une paire d’électrons ou donner un ion hydrogène ou un proton dans une réaction chimique, tandis que les bases peuvent donner une paire d’électrons ou accepter un hydrogène ou un proton.
- Les acides et les bases sont caractérisés comme étant forts ou faibles. Un acide fort ou une base forte se dissocie complètement en ses ions dans l’eau. Si le composé ne se dissocie pas complètement, il s’agit d’un acide ou d’une base faible. Le degré de corrosivité d’un acide ou d’une base n’est pas lié à sa force.
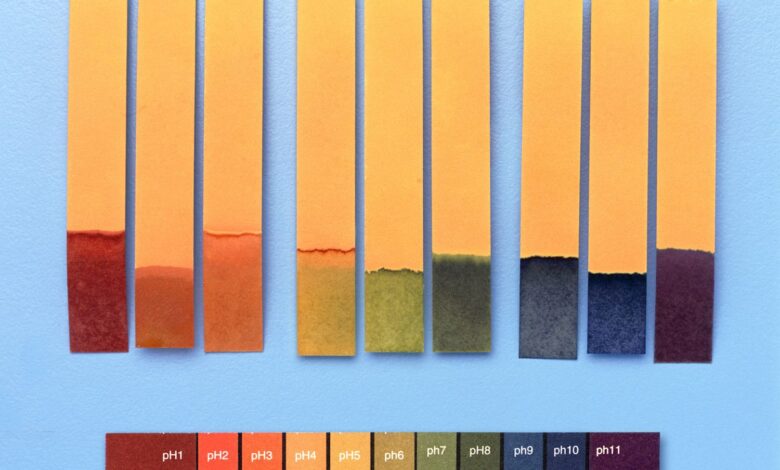
- L’échelle de pH est une mesure de l’acidité ou de l’alcalinité (basicité) ou d’une solution. L’échelle va de 0 à 14, les acides ayant un pH inférieur à 7, 7 étant neutre, et les bases ayant un pH supérieur à 7.
- Les acides et les bases réagissent entre eux dans ce que l’on appelle une réaction de neutralisation. Cette réaction produit du sel et de l’eau et laisse la solution plus proche d’un pH neutre qu’auparavant.
- Un test courant pour savoir si un inconnu est un acide ou une base est de mouiller du papier de tournesol avec. Le papier de tournesol est un papier traité avec un extrait d’un certain lichen qui change de couleur en fonction du pH. Les acides rendent le papier de tournesol rouge, tandis que les bases le rendent bleu. Un produit chimique neutre ne changera pas la couleur du papier.
- Parce qu’ils se séparent en ions dans l’eau, les acides et les bases conduisent l’électricité.
- Bien que l’on ne puisse pas dire si une solution est un acide ou une base en la regardant, le goût et le toucher peuvent être utilisés pour les distinguer. Cependant, comme les acides et les bases peuvent être corrosifs, vous ne devez pas tester les produits chimiques en les goûtant ou en les touchant ! Les acides et les bases peuvent provoquer une brûlure chimique. Les acides ont tendance à avoir un goût aigre et à être secs ou astringents, tandis que les bases ont un goût amer et sont glissantes ou savonneuses. Le vinaigre (acide acétique faible) et la solution de bicarbonate de soude (bicarbonate de soude dilué – une base) sont des exemples d’acides et de bases ménagères que vous pouvez tester.
- Les acides et les bases sont importants dans le corps humain. Par exemple, l’estomac sécrète de l’acide chlorhydrique, HCl, pour digérer les aliments. Le pancréas sécrète un liquide riche en bicarbonate de base pour neutraliser l’acide de l’estomac avant qu’il n’atteigne l’intestin grêle.
- Les acides et les bases réagissent avec les métaux. Les acides libèrent du gaz hydrogène lorsqu’ils réagissent avec les métaux. Parfois, de l’hydrogène gazeux est libéré lorsqu’une base réagit avec un métal, par exemple en faisant réagir de l’hydroxyde de sodium (NaOH) et du zinc. Une autre réaction typique entre une base et un métal est une réaction de double déplacement, qui peut produire un précipité d’hydroxyde de métal.
Caractéristique
Acides
Bases
Réactivité
accepter des paires d’électrons ou donner des ions d’hydrogène ou des protons
donner des paires d’électrons ou donner des ions hydroxyde ou des électrons
pH
moins de 7
supérieur à 7
le goût (ne testez pas les inconnues de cette façon)
aigre
savonneux ou amer
corrosivité
peut être corrosif
peut être corrosif
toucher (ne pas tester les inconnues)
astringent
glissante
test décisif
rouge
bleu
conductivité en solution
conduire l’électricité
conduire l’électricité
exemples courants
vinaigre, jus de citron, acide sulfurique, acide chlorhydrique, acide nitrique
eau de Javel, savon, ammoniaque, hydroxyde de sodium, détergent
Tableau comparatif des acides et des bases