Contents
La science de la physique étudie les objets et les systèmes afin de mesurer leurs mouvements, leurs températures et d’autres caractéristiques physiques. Elle peut s’appliquer à tout, des organismes unicellulaires aux systèmes mécaniques, en passant par les planètes, les étoiles et les galaxies, ainsi que les processus qui les régissent. En physique, la thermodynamique est une branche qui se concentre sur les changements d’énergie (chaleur) dans les propriétés d’un système au cours de toute réaction physique ou chimique.
Le « processus isotherme », qui est un processus thermodynamique dans lequel la température d’un système reste constante. Le transfert de chaleur dans ou hors du système se fait si lentement que l’équilibre thermique est maintenu. « Thermique » est un terme qui décrit la chaleur d’un système. « Iso » signifie « égal », donc « isotherme » signifie « chaleur égale », ce qui définit l’équilibre thermique.
Le processus isotherme
En général, au cours d’un processus isotherme, il y a une modification de l’énergie interne, de l’énergie thermique et du travail, même si la température reste la même. Quelque chose dans le système fonctionne pour maintenir cette température égale. Un exemple idéal simple est le cycle de Carnot, qui décrit essentiellement comment un moteur thermique fonctionne en fournissant de la chaleur à un gaz. En conséquence, le gaz se dilate dans un cylindre, et cela pousse un piston à faire du travail. La chaleur ou le gaz doit ensuite être poussé hors du cylindre (ou déchargé) pour que le cycle chaleur/expansion suivant puisse avoir lieu. C’est ce qui se passe à l’intérieur d’un moteur de voiture, par exemple. Si ce cycle est totalement efficace, le processus est isotherme car la température est maintenue constante alors que la pression change.
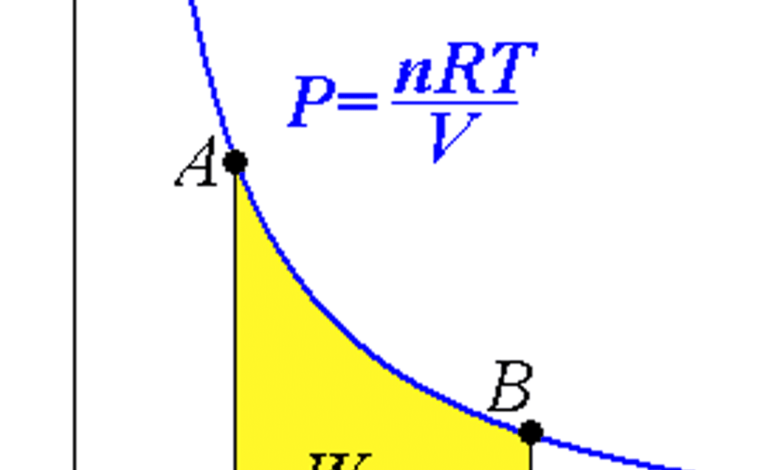
Pour comprendre les bases du processus isotherme, il faut considérer l’action des gaz dans un système. L’énergie interne d’un gaz idéal dépend uniquement de la température, de sorte que la variation de l’énergie interne au cours d’un processus isotherme pour un gaz idéal est également de 0. Dans un tel système, toute la chaleur ajoutée à un système (de gaz) effectue un travail pour maintenir le processus isotherme, tant que la pression reste constante. Essentiellement, lorsque l’on considère un gaz idéal, le travail effectué sur le système pour maintenir la température signifie que le volume du gaz doit diminuer à mesure que la pression sur le système augmente.
Procédés isothermes et états de matière
Les processus isothermes sont nombreux et variés. L’évaporation de l’eau dans l’air en est un, tout comme l’ébullition de l’eau à un point d’ébullition spécifique. Il existe également de nombreuses réactions chimiques qui maintiennent l’équilibre thermique et, en biologie, les interactions d’une cellule avec les cellules qui l’entourent (ou d’autres matières) sont considérées comme un processus isotherme.
L’évaporation, la fusion et l’ébullition sont également des « changements de phase ». Autrement dit, ce sont des changements de l’eau (ou d’autres fluides ou gaz) qui se produisent à température et pression constantes.
Cartographie d’un processus isotherme
En physique, la représentation graphique de ces réactions et processus se fait à l’aide de diagrammes (graphiques). Dans un diagramme de phase, un processus isotherme est représenté en suivant une ligne verticale (ou un plan, dans un diagramme de phase en 3D) le long d’une température constante. La pression et le volume peuvent changer afin de maintenir la température du système.
Lorsqu’elles changent, il est possible pour une substance de changer son état de matière même si sa température reste constante. Ainsi, l’évaporation de l’eau en ébullition signifie que la température reste la même alors que le système change de pression et de volume. La température reste alors constante le long du diagramme.
Ce que tout cela signifie
Lorsque les scientifiques étudient les processus isothermes dans les systèmes, ils examinent réellement la chaleur et l’énergie et le lien entre celles-ci et l’énergie mécanique nécessaire pour modifier ou maintenir la température d’un système. Cette compréhension aide les biologistes à étudier comment les êtres vivants régulent leur température. Elle entre également en jeu dans l’ingénierie, la science spatiale, la science planétaire, la géologie et de nombreuses autres branches scientifiques. Les cycles de puissance thermodynamiques (et donc les processus isothermes) sont l’idée de base des moteurs thermiques. Les humains utilisent ces dispositifs pour alimenter des centrales électriques et, comme mentionné ci-dessus, des voitures, des camions, des avions et d’autres véhicules. En outre, de tels systèmes existent sur les fusées et les vaisseaux spatiaux. Les ingénieurs appliquent les principes de la gestion thermique (en d’autres termes, la gestion de la température) pour accroître l’efficacité de ces systèmes et processus.
Édité et mis à jour par Carolyn Collins Petersen.